2014 a été déclarée année internationale de la cristallographie par l’UNESCO. La Fête de la science qui se déroule chaque année en France a, évidemment, le même thème. Comment animer des activités pour enfants, jeunes et adultes sur la cristallographie ?
Le choix de l’UNESCO est justifiée par le croissant intérêt, surtout pour ce qui concerne l’importance des applications, de cette discipline trop peu connue.
Commençons par comprendre les grands traits : qu’est-ce que c’est un cristal et comment il se forme, avec des exemples et des activités pratiques.
Comment se forme un cristal ?
La première chose qui me vient à l’esprit, et qui est un grand classique, est de créer des cristaux “fait maison” avec des matériaux de tous les jours pour voir comment ils se forment et les observer de près (si possible avec une loupe binoculaire ou au moins avec une loupe normale).
Étant donné qu’un cristal de sel ou de sucre met quelques jours à se former, la cristallisation n’est pas très intéressante comme expérience si l’activité avec le public dure une heure/une heure et demie. Par contre c’est intéressant dans une classe où les élèves peuvent voir la progression jour après jour.
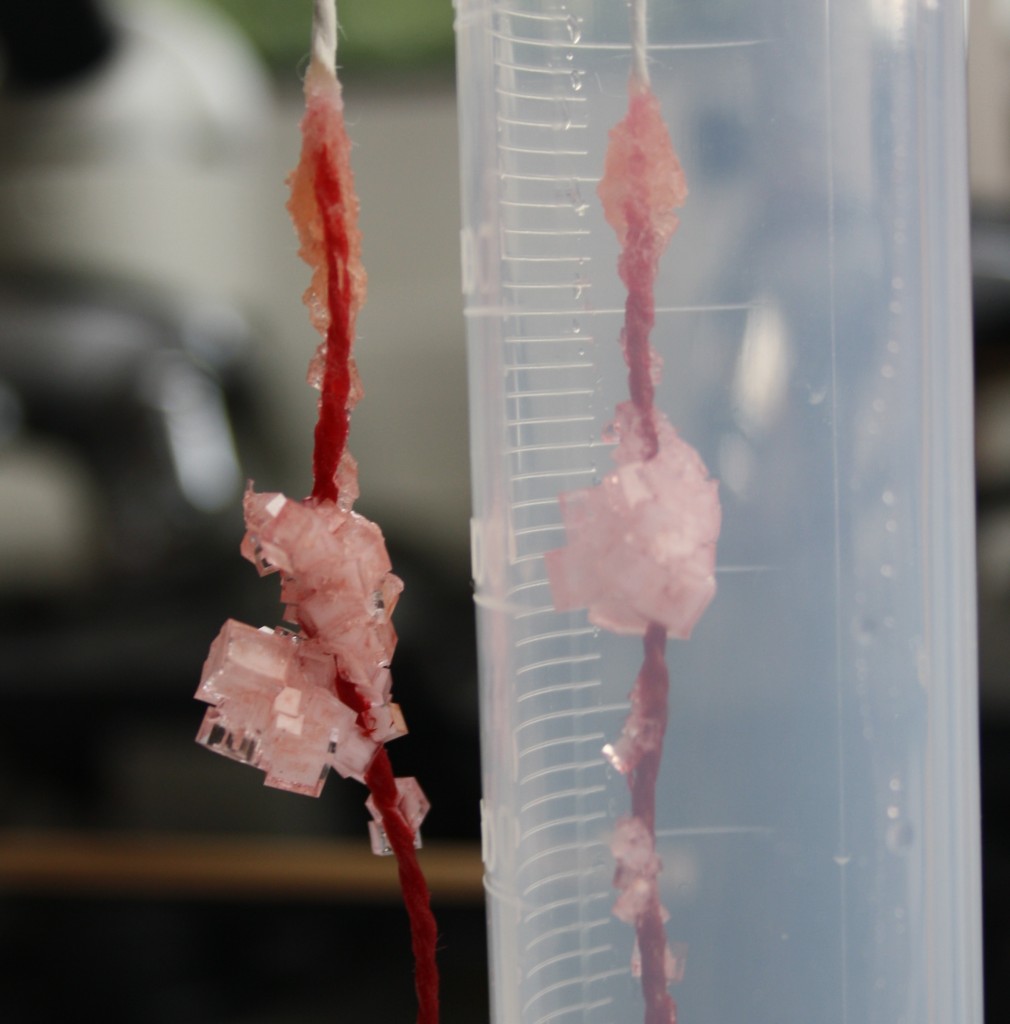
Mais comment se forme un cristal ? Il existe différentes modalités, mais la plus facile à expliquer et à observer en un temps non géologique est la précipitation. Le concept est simple : une solution sursaturée de soluté le fait précipiter sous forme de cristal. Par exemple une solution contenant entre 250 g et 350 g de sel de cuisine dissous dans 1 litre d’eau bouillante cristallise en deux ou trois jours si on en met une couche fine dans une assiette plate ou une boîte de Pétri (voir photo). Si on plonge un fil dans la même solution, les cristaux vont se superposer en formant une espèce de cordelette de cristaux, mais il faudra plusieurs semaines.

Et voilà le résultat.
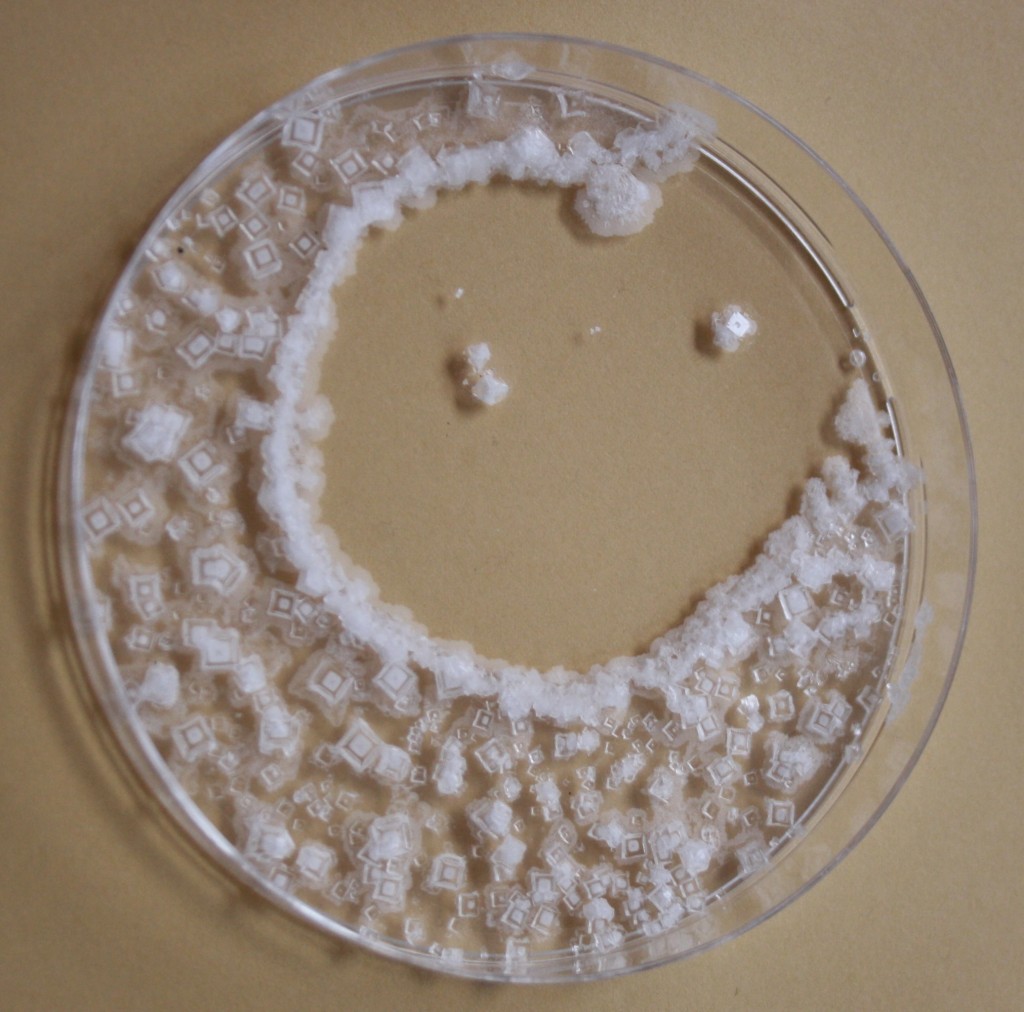


La cristallisation d’une solution de sucre (saccharose) est beaucoup plus lente. On peut en outre observer que les cristaux de sel sont cubiques et ceux de sucre non. Ça devrait soulever des questions et stimuler la curiosité.
Pourquoi les cristaux ont des formes géométriques ?
Pour connaître nous utilisons les sens. Depuis l’antiquité les hommes sont attirés par les cristaux parce que ils sont agréables à voir. Mais pourquoi sont-ils beaux ? Nous aimons les cristaux parce que ils sont colorés, translucides, brillants mais surtout parce qu’ils ont des précises formes géométriques. Montrer explicitement la correspondance entre la forme des cristaux et des maquettes tridimensionnelles de solides peut donner une clé de lecture ou du moins suggérer un regard différent.



Comment ça se fait que les cristaux ont ces formes régulières ?Pour chercher une réponse il faut rechercher la relation entre la forme extérieure et la structure intérieure.
Les atomes, les molécules ou les ions (les petites parties qui composent le cristal) n’occupent pas des positions au hasard mais ils sont organisés de manière parfaitement ordonnée et périodique dans l’espace qui détermine des figures géométriques à niveau macroscopique.
Un peu comme les petites boules de cette photo qui occupent des positions ordonnées et qui forment, selon le cas, un parallélépipède ou une pyramide.

La position des atomes est déterminée par la nature chimique du cristal (distance entre les atomes, type de lien, charge électrique, géométrie moléculaire, etc.) et aussi par l’exigence de compacité de la structure formée. Les atomes se positionnent de façon à occuper le moindre espace possible et à occuper les interstices.
Une structure très compacte est la pyramide. C’est pour ça qu’on retrouve cette structure sur les stands des maraîchers et dans les dépôts de boulets de canon.

Naturellement le sujet est bien plus complexe, Je n’ai pas la prétention de donner une explication exhaustive. Qui veut peut approfondir avec des activités sur la géométrie et les maths (par ex. parler des nombres pyramidaux). D’après mon expérience je peux dire que la construction de la pyramide plaît beaucoup !
Il n’existe pas que des cristaux qui ont une belle forme géométrique et des faces lisses et brillantes. D’autres cristaux sont comme des petits grains de sable mélangés ensemble. Ça arrive parce que ils n’ont pas eu l’espace pour s’accroître mais ils se sont superposés les uns aux autres en empêchant le développement d’une belle forme.
Il existe en outre des solides non cristallins, c’est à dire des solides où les atomes n’ont pas des positions ordonnées, par exemple le verre et certains types de plastique. Parfois ces substances ne sont pas considérées comme des solides mais plutôt comme des liquides avec une viscosité très élevée.
On peut affirmer qu’un cristal est une formation solide, mais je préfère la définition de cristal comme un état de la matière. Ça introduit le concept que même des “objets” qui normalement ne sont pas solides (comme les protéines, l’ADN, etc.) peuvent être cristallisés sous certaines conditions.
Et c’est ça qui a rendu possible l’utilisation des techniques de cristallographie pour l’étude de la biologie. Parce que la cristallographie n’est pas seulement l’étude des cristaux, mais également une technique qui permet, grâce à la diffraction des rayons X à travers une substance cristallisée, de remonter à la structure moléculaire de la substance analysée.
On irradie un cristal avec des rayons X et on regarde comment ceux-ci se diffractent (passent à travers et sont déviés) sur une plaque photographique. À l’inverse, on peut partir par le résultat obtenu par la diffraction d’une substance cristallisée sur la plaque pour en déduire sa structure.
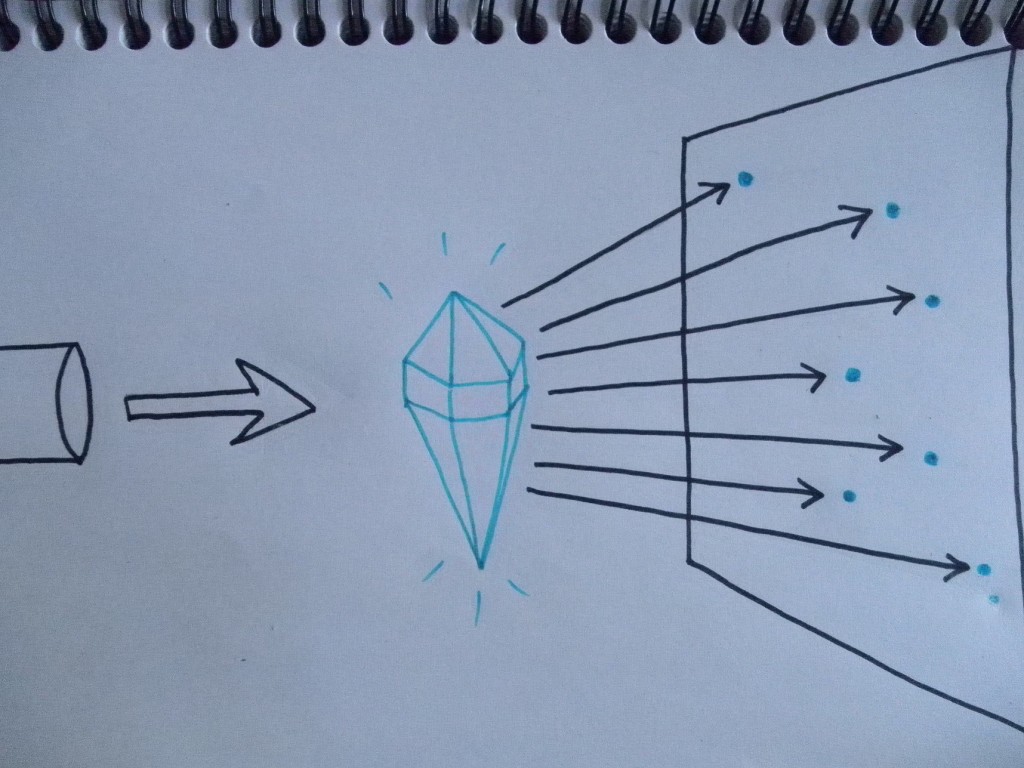
Cette année c’est le centenaire de cette découverte considérée à présent l’outil le plus puissant pour l’étude de la structure de la matière. Vingt-trois prix Nobel liés à la cristallographie ont déjà été assignés. Par exemple celui du 1962 attribué à Watson, Crick et Wilkins pour la découverte de la structure à double hélice de l’ADN, avec la contribution fondamentale de Rosalind Franklin, sous forme d’une photographie réalisée avec la techniques de la cristallographie à rayons X. Je parlerai de Rosalind Franklin dans un autre article.
En résumant: les explications sur la cristallographie à rayons X je les utiliserais avec un public pas trop jeunes; pour ce qui concerne les activités pratiques (que j’ai testées à partir de 8 ans) on peut faire pousser et observer des cristaux de sel et de sucre, toucher (et peser, et sentir !) des minéraux et les regarder à la loupe binoculaire, construire des maquettes de cristaux avec plusieurs matériaux et, pourquoi pas, fabriquer quelques paper toy en forme de cristaux comme ceux dans la photo en bas.
Amusez-vous bien et bonne année de la cristallographie !
Paper toys
Pour aller plus loin
Patrons à télécharger pour les paper toys
Si vous voulez essayer la recette des sucettes cristallines (moi je n’ai pas eu des bons résultats mais je dois re-essayer…) cliquer ici
Un peu d’info
en français
http://www.aicr2014.fr/index.php/pourquoi-l-annee-cristallo
http://www.kasuku.ch/pdf/cristallographie/cristallographie.pdf
http://kidiscience.cafe-sciences.org/articles/experience-a-la-maison-comment-faire-pousser-du-sel/
en italien
http://www.uniroma2.it/didattica/STM_ENE/deposito/Lezione__2_struttura_cristallina._pptx.pdf
https://sites.google.com/site/cristallografia/
http://www.chimicamo.org/chimica-generale/solidi-molecolari-e-loro-struttura.html






Cela me donne envie de tenter les cristaux de sucre à nouveau!!
Fais nous connaître les résultats !
Bonjour,
Merci pour cet article très riche !
Nous avons fait pousser avec succès différents cristaux avec mon fils : sucre, sel, acide citrique (très beau !). Je suis complètement novice et cela m’a suscité une question, que je n’arrive pas à résoudre dans les livres ou sites existants et qui me bloque pour la suite : nos cristaux de sel et de sucre sont constitués d’une même forme (un cube) qui se multiplie (les cubes de sel sont séparés les uns des autres, ceux de sucre sont agglomérés). Pourtant, on voit souvent des cristaux dont la forme initiale grossit. D’ailleurs Wikipédia indique que la croissance des cristaux « (…) est caractérisée par l’empilement à la surface du cristal de nouvelles particules qui se logent dans des sites préférentiels » Alors pourquoi nos cristaux se multiplient au lieu de grossir ?
Merci beaucoup par avance pour votre aide précieuse ! Et pour cet article qui donne plein de pistes pour poursuivre nos expérimentations 🙂
Bonjour, merci beaucoup pour votre message. J’avoue que je ne sais pas répondre à votre question mais je vais me renseigner. A bientôt !